在糖尿病的诊断和治疗中,我们习惯于“非此即彼”的二分法:要么是1型糖尿病(T1DM),要么是2型糖尿病(T2DM)。然而,在临床实践中,总有一些案例令医生困惑:一些起病时看似患有“2型糖尿病”的成年患者,很快就进展为胰岛素依赖;有些患者在发病时看似患有“2型糖尿病”,但很快就发展为胰岛素依赖;有些患者已接受2型糖尿病治疗多年,但在某种感染或压力后出现酮症倾向。这些病例的背后隐藏着一种长期被低估的糖尿病——成人潜伏性自身免疫性糖尿病(LADA)。
1. LADA:被忽视的“中间地带”血糖分析仪
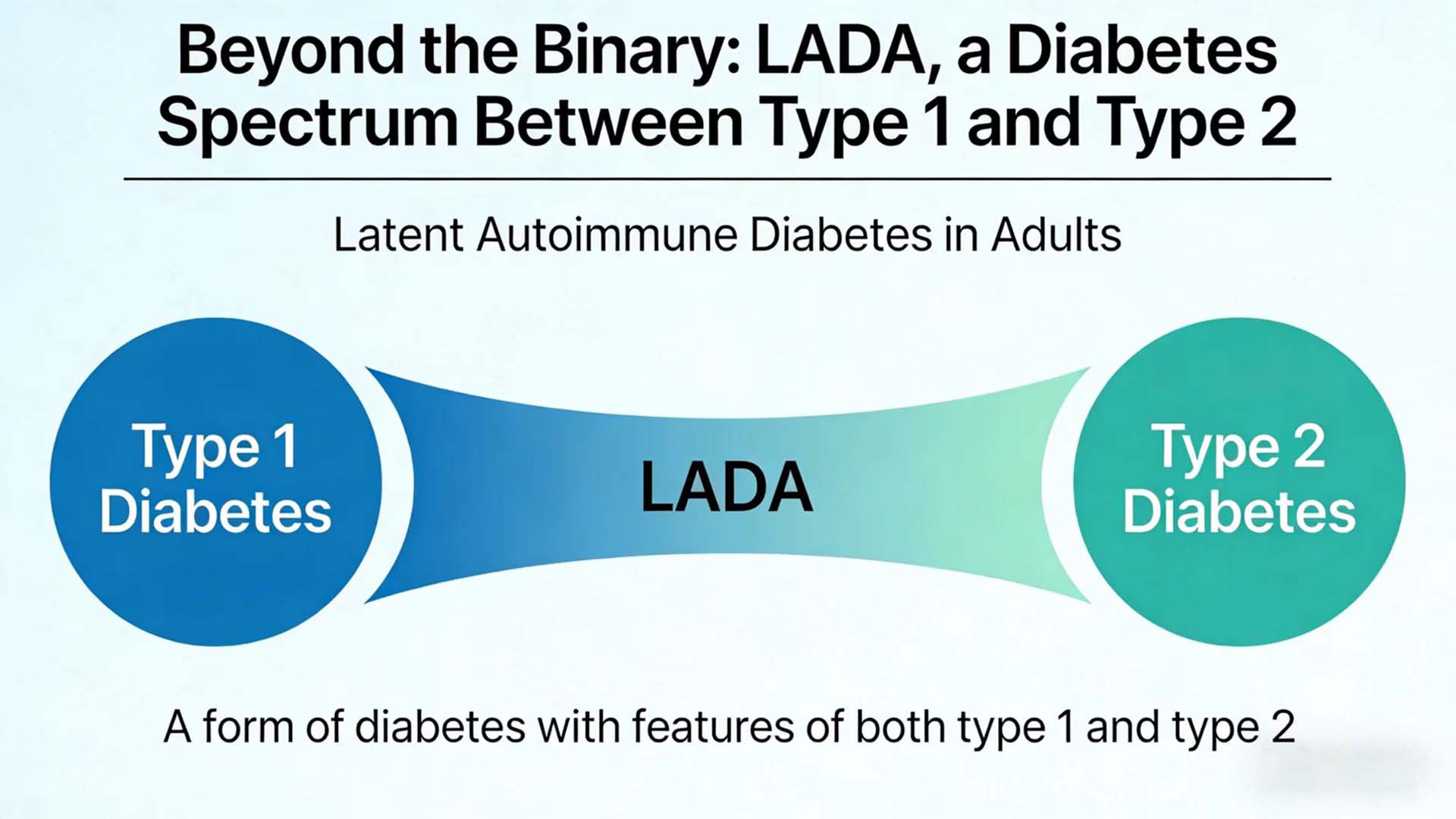
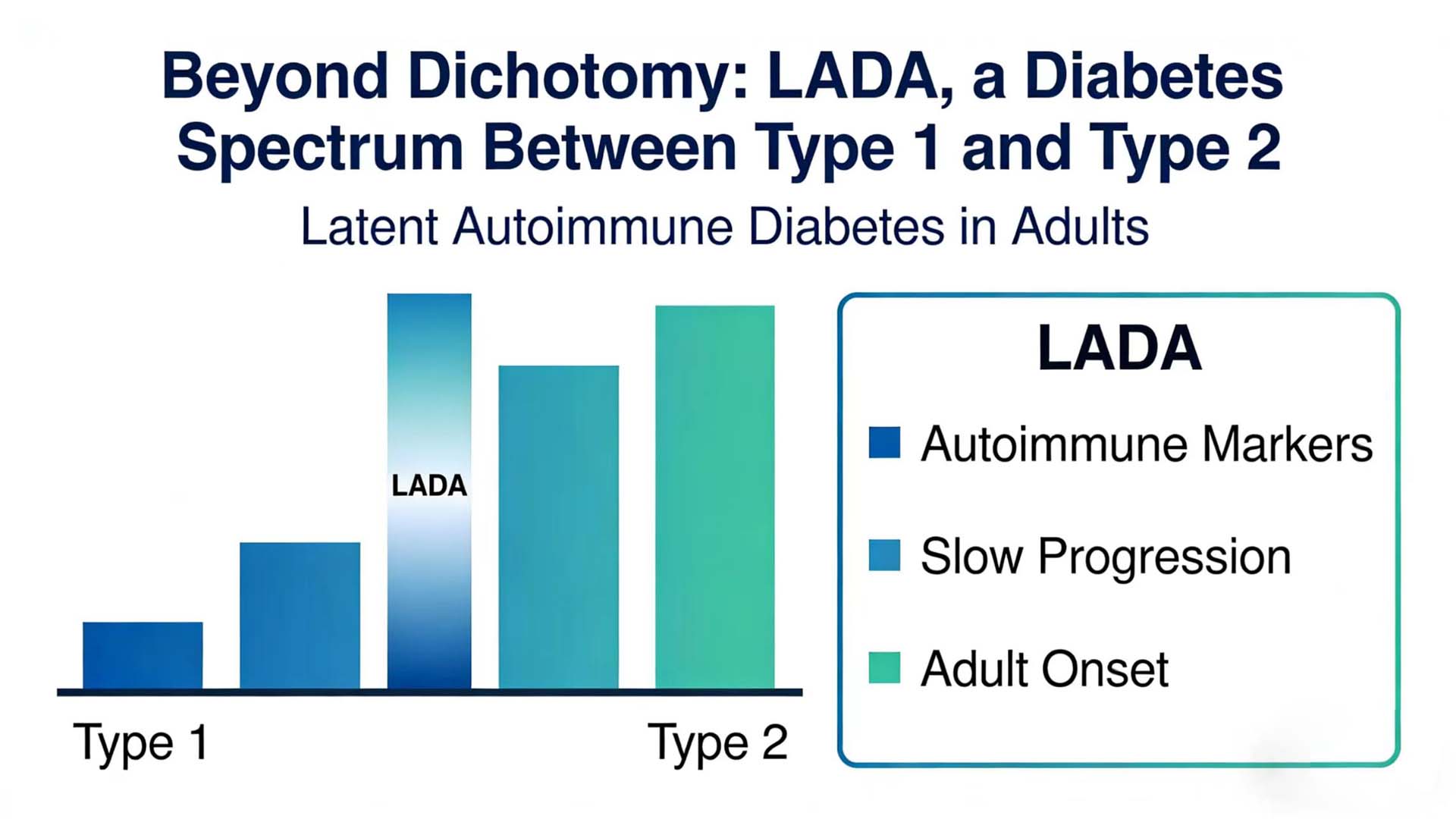
LADA是一种特殊类型的糖尿病,介于1型和2型糖尿病之间,结合了两者的特征,但并不完全属于任何一种类型。近年来,随着对自身免疫机制认识的加深和检测技术的进步,LADA的诊疗模式正在经历从“经验诊断”到“精准分类”的深刻转变。
1.1 定义与分类:从“隐藏”到“动态”的认知演化
LADA是指发病年龄≥18岁(或30岁,不同指南标准略有差异)的一类糖尿病,发病时无明显酮症倾向,但有胰腺β细胞自身免疫损伤的证据。其核心特征在于其“阴险”本质——发病时的临床表现与2型糖尿病相似,但自身免疫过程不断进展,最终大多数患者将依赖胰岛素治疗。
国际糖尿病联盟 (IDF) 和美国糖尿病协会 (ADA) 尚未将 LADA 列为独立分类。但在临床实践中,根据自身抗体是否阳性,成人糖尿病可简化为“自身免疫阳性”(包括1A型糖尿病和LADA)和“自身免疫阴性”(主要是T2DM)。 LADA与1A型糖尿病的主要区别在于发病年龄、发病方式和β细胞功能衰退速度:前者发病较晚,进展较慢,而后者多见于儿童和青少年,起病急,β细胞功能衰竭较快。
近年来,学者进一步提出了LADA“分型”的概念:根据发病年龄(如≤35岁与>35岁)和抗体阳性数量(如单项抗体阳性与抗体阳性),根据多种抗体阳性和β细胞功能残留程度(如C肽水平)等因素将LADA分为“缓慢进展型”和“快速进展型”。这种分类对于LADA的诊断具有重要的指导意义。选择治疗策略——例如,多种抗体阳性且C肽水平低的患者可以更早开始胰岛素治疗。
1.2 流行病学数据:被低估的“冰山一角”
成人糖尿病中 LADA 的患病率因诊断标准的不同,特别是年龄临界值和抗体检测的结合而有所不同,但一般在 10% 至 25% 之间。 LADA中国研究显示,18岁以上初诊糖尿病患者中,GADAb阳性率为5.9%-12.6%。若结合IA-2Ab检测,阳性率可提高至8%-10%。
值得注意的是,LADA的患病率随着发病年龄的增加而降低:在18~30岁的新诊断糖尿病患者中,LADA约占20%。在60岁以上的人群中,仍占5%至10%。这提醒我们,即使是中老年糖尿病患者,自身免疫因素也不容忽视。此外,LADA患者常存在代谢异常(如肥胖和血脂异常),但肥胖程度通常低于T2DM患者。而且,腰围、BMI等指标与抗体滴度呈负相关,即体形越瘦、代谢紊乱越轻微,自身免疫损害可能越突出。
1.3 临床意义:为什么早期识别 LADA 至关重要?血糖套件
LADA的误诊或漏诊会导致治疗策略的偏差,影响患者的预后。一方面,如果LADA被误诊为T2DM,长期使用胰岛素增敏剂(如二甲双胍)或分泌剂(如磺脲类药物)可能无法有效延缓β细胞功能衰退,甚至可能加速其衰竭。另一方面,LADA患者发生心血管并发症、微血管病变(如糖尿病肾病、视网膜病变)、神经病变的风险显着高于T2DM患者,这可能与慢性高血糖、自身免疫炎症、胰岛素分泌不足共同相关。
早期识别LADA的意义不仅在于纠正治疗方案,还在于为患者提供“个体化预警”。例如,明确诊断LADA后,需要加强血糖监测,避免可能引发酮症的因素(如感染、压力),并早期筛查糖尿病并发症。此外,LADA作为自身免疫性糖尿病的“中间型”,为研究1A型糖尿病发病机制提供了天然模型,有利于探索免疫干预的“时间窗口”。
2. LADA发病机制:遗传、免疫和环境的“三角博弈”
LADA发病机制复杂,涉及遗传、免疫、环境等多种因素相互作用,形成复杂的“三角博弈”。
2.1 遗传背景:易感基因的“双重作用”
LADA的遗传易感性结合了1A型糖尿病和2型糖尿病的特点。其中人类白细胞抗原(HLA)基因是最重要的遗传因素,尤其是HLA-DR/DQ位点的多态性。与1A型糖尿病相似,LADA患者HLA-DR3、DR4及其杂合子(DR3/DR4)的频率显着增加。然而,与1A型不同的是,LADA患者中HLA-DR2的频率降低,而HLA-DR9(亚洲人群中常见)的频率升高——这可能是亚洲人群中LADA高发的遗传基础。
非 hla 基因也参与 LADA 的发病机制。 PTPN22基因编码的淋巴磷酸酶可通过调节T细胞活化影响自身免疫反应,其rs2476601多态性(R620W)与LADA风险相关。 CTLA-4基因(免疫调节关键基因)的rs231775多态性也与LADA的易感性相关。此外,T2DM易感基因(如TCF7L2和KCNJ11)在LADA患者中也存在突变,提示遗传背景的“叠加效应”可能决定LADA的临床表型。
2.2 自身免疫:从“发起”到“攻击”的级联反应
LADA的核心病理生理特征是胰腺β细胞的自身免疫损伤,这一过程与1A型糖尿病相似,但进展较慢。目前认为,LADA的自身免疫反应始于触发它的环境因素(如病毒感染、饮食因素),这些因素激活遗传易感个体中的抗原呈递细胞(如树突状细胞)。随后,激活的CD4+T细胞协助B细胞产生自身抗体(如GADAb、IA-2Ab),而CD8+T细胞则直接杀伤β细胞。
自身抗体是LADA免疫损伤的“标志物”,也是临床诊断的核心依据。其中谷氨酸脱羧酶抗体(GADAb)灵敏度最高(90%以上),持续时间最长。胰岛抗原2抗体(IA-2Ab)、胰岛素自身抗体(IAA,年轻患者多见)、锌转运蛋白8抗体(ZnT8Ab)阳性率依次下降。多种抗体联合检测可以提高LADA的检出率——例如GADAb和IA-2Ab抗体同时阳性者,β细胞功能衰退速度较快,五年内胰岛素依赖率可达80%。
2.3 环境因素:引发免疫力的“最后一根稻草”
环境因素在LADA发病机制中的作用尚不完全清楚,但目前认为可能涉及“卫生学假说”和“分子模拟假说”。 “卫生假说”认为,儿童时期感染的减少(例如过度清洁和滥用抗生素)可能会导致免疫系统过度激活,容易攻击自身组织。 “分子模拟假说”认为,某些病毒(如柯萨奇病毒、流行性腮腺炎病毒)的抗原成分与β细胞抗原相似,感染后激活的T细胞可能“意外损伤”β细胞。
此外,肠道菌群失调可能通过“肠胰轴”参与LADA的发病机制。研究发现,LADA患者肠道菌群多样性降低,产生短链脂肪酸的细菌(如普拉蒂斯梭菌)减少,致病菌(如肠杆菌科)增加。微生物群的代谢产物(如脂多糖)可能通过 Toll 样受体激活胰岛的局部炎症反应,并加速 β 细胞损伤。血糖测量
3. LADA的诊断:从“经验判断”到“免疫标志物联合验证”
早期诊断是LADA管理的关键。随着检测技术的进步,LADA的诊断已从“经验判断”转向“免疫标志物联合验证”。
3.1 诊断标准:从“单一指标”到“综合判断”
根据《中国成人隐匿性自身免疫性糖尿病诊治专家共识(2021年版)》,LADA的诊断标准为:
发病年龄≥18岁。
胰岛自身抗体阳性或胰岛自身免疫T细胞阳性;
诊断糖尿病后至少半年内不应依赖胰岛素治疗。
与旧版共识相比,新版共识将胰腺自身免疫T细胞阳性纳入诊断标准,有助于识别抗体阴性但自身免疫损伤的患者。此外,新共识建议对所有新诊断的T2DM患者进行谷氨酸脱羧酶自身抗体(GADA)筛查。对于GADA抗体阴性的患者,如果临床怀疑患有LADA,应进一步筛查其他自身抗体或胰岛抗原特异性T细胞。
3.2 诊断路径:从“被动发现”到“主动筛查”
新共识推荐的LADA诊断路径为:
对所有新诊断的 T2DM 患者进行了 GADA 常规筛查。
对于GADA阳性的患者,结合发病年龄和胰岛素依赖性来诊断LADA。
对于GADA阴性但临床怀疑LADA的患者(如有1型糖尿病家族史、BMI诊断为LADA的患者,应进一步评估胰腺β细胞功能、自身抗体滴度和合并症),以指导治疗决策。血糖测量
3.3 鉴别诊断:避免“非此即彼”的误解
LADA的鉴别诊断主要包括:
1A型糖尿病:发病年龄通常小于30岁,发病急性。常伴有酮症酸中毒、胰腺β细胞功能快速衰竭、自身抗体阳性率较高。
2型糖尿病:起病隐袭,常表现为肥胖、胰岛素抵抗等代谢综合征表现。自身抗体呈阴性,β细胞功能下降缓慢。
其他特殊类型的糖尿病,如线粒体糖尿病和MODY,可以通过基因检测等手段来识别。
4. LADA治疗:从“控制血糖”到“保护β细胞”的策略升级
LADA的治疗目标不仅是控制血糖,更重要的是调节胰岛的自身免疫反应,保护胰腺β细胞的功能,预防糖尿病并发症和合并症。
4.1 治疗原则:个体化、分层管理
根据《中国成人隐匿性自身免疫性糖尿病诊治专家共识(2021年版)》,LADA治疗应根据C肽水平、GADA滴度和合并症情况进行个体化、分层治疗。
如果C肽小于0.3 nmol/L或GADA滴度≥180 U/ml:建议胰岛素治疗。
如果C肽≥0.3 nmol/L且GADA滴度为
4.2 药物选择:避有害,选有益
LADA药物的选择应遵循以下原则:
避免使用磺酰脲类药物:磺酰脲类药物会刺激胰腺β细胞分泌胰岛素,可能会加速β细胞功能的衰竭。
胰岛素治疗:对于胰岛功能较差、GADA滴度较高的患者,应尽早使用胰岛素治疗,以保护残余的β细胞功能。
口服降糖药物:对于胰岛功能良好、GADA滴度较低的患者,可选用二甲双胍、DPP-4抑制剂、GLP-1受体激动剂、SGLT2抑制剂等药物,但应避免磺脲类药物。
免疫调节治疗:目前免疫调节治疗还处于研究阶段,如维生素D、免疫抑制剂等,可能对胰岛功能有一定的保护作用,但还需要进一步验证。
4.3 生活方式干预:基础中的基础
生活方式干预是LADA治疗的基础,包括饮食控制、适度运动、体重管理、戒烟限酒等。研究表明,健康的生活方式可以改善胰岛素抵抗,减轻胰腺β细胞的负担,延缓病情进展。
5、未来展望:迈向LADA“精准医疗”时代
随着医疗技术的不断进步,LADA的诊断和治疗将面临更多的机遇和挑战
精准分型:通过基因检测、代谢组学、蛋白质组学等技术,进一步完善LADA分型,为个体化治疗提供依据。
早期筛查:开发更灵敏、特异的自身抗体检测方法,或利用人工智能技术分析临床数据,实现LADA的早期筛查和诊断。
免疫治疗:探索针对LADA的特异性免疫治疗方法,如抗原特异性免疫耐受、免疫细胞治疗等,以预防或逆转自身免疫损伤。
β细胞再生:研究干细胞移植、基因编辑等β细胞再生技术,为LADA患者提供新的治疗选择。
LADA 是一种特殊类型的糖尿病,介于 1 型和 2 型糖尿病之间,挑战了我们对糖尿病“非此即彼”的二分法理解。随着我们对LADA认识的加深,我们逐渐意识到糖尿病并不是简单的“1型”或“2型”,而是一个连续的疾病谱,而LADA就是这个谱的重要组成部分。
早期识别、精准分类、个体化治疗是LADA管理的关键。作为临床医生,我们需要打破“非此即彼”的思维定势,关注糖尿病的“非典型”病例,通过免疫标志物检测等手段早期发现LADA患者,并根据其临床特征和病情进展制定个体化治疗方案。
未来,随着精准医疗技术的不断发展,我们有望实现LADA的早期筛查、精准诊断和有效治疗,为这一特殊人群带来更好的健康结果。让我们超越二分法,重新认识糖尿病的疾病谱,为LADA患者提供更精准、更有效的医疗服务。
发布时间:2026年2月9日